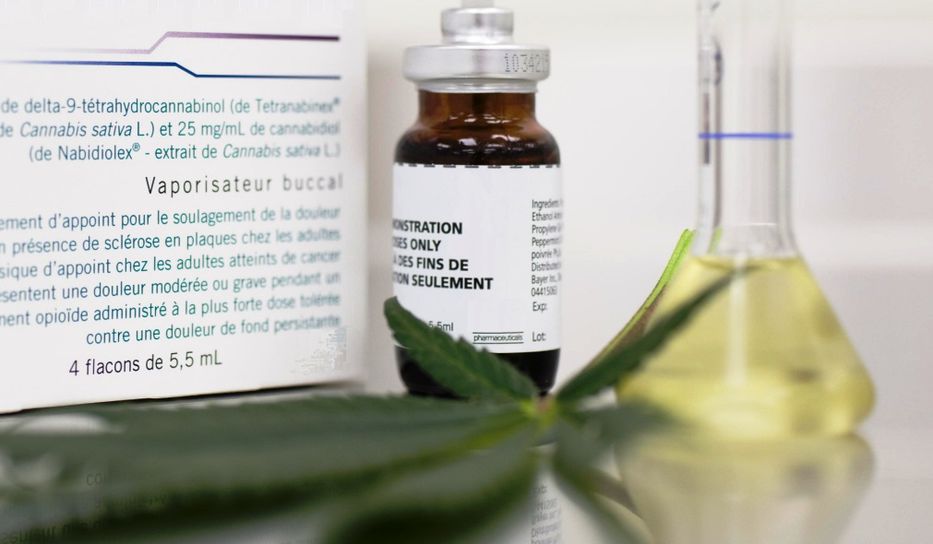
Fue registrado bajo el nombre específico de Mevatyl (tetraidrocanabinol (THC), 27 mg/mL + canabidiol (CBD), 25 mg/mL), y está compuesto por canabinoides obtenidos a partir de Cannabis sativa. Se presenta en forma de solución oral (spray), según reporta Anvisa.
El nuevo medicamento está registrado en otros países con el nombre comercial Sativex, y está indicado para el tratamiento sintomático de espasticidad moderada severa relacionada con la esclerosis múltiple, y está destinado a pacientes adultos que no responden a otros medicamentos antiespásticos que muestran una mejoría clínicamente significativa en los síntomas relacionados durante el periodo inicial.
El fármaco está diseñado para usarse como complemento de la medicación antiespasmódica actual del paciente y está aprobado en otros 28 países, entre ellos Canadá, EE.UU., Alemania, Dinamarca, Suecia, Suiza e Israel.
En el caso del medicamento, que se fabrica en Reino Unido, Anvisa asegura que está demostrado que ofrece una mejoría "clínicamente significativa" en los espasmos causados por la esclerosis múltiple y que su dependencia es "poco probable". No obstante, la droga no es recomendada para uso en niños y adolescentes menores de 18 años de edad debido a la falta de datos de seguridad y eficacia para los pacientes en este grupo de edad.

Acerca de los comentarios
Hemos reformulado nuestra manera de mostrar comentarios, agregando tecnología de forma de que cada lector pueda decidir qué comentarios se le mostrarán en base a la valoración que tengan estos por parte de la comunidad. AMPLIAREsto es para poder mejorar el intercambio entre los usuarios y que sea un lugar que respete las normas de convivencia.
A su vez, habilitamos la casilla [email protected], para que los lectores puedan reportar comentarios que consideren fuera de lugar y que rompan las normas de convivencia.
Si querés leerlo hacé clic aquí[+]